서론
수술중신경계감시(intraoperative neurophysiologic monitoring, IONM)는 수술 중에 발생할 수 있는 신경 손상을 전기생리학적 검사를 이용하여 실시간으로 감시하여 신경학적 합병증을 줄이는 데 도움이 된다고 알려져 있으며, 척추수술 분야에서 그 유용성이 보고된 바 있다. IONM에서는 수술 중에 나타날 수 있는 신경생리학적 변화를 감지하기 위하여 운동유발전위(motor evoked potential, MEP)와 체성감각유발전위(somatosensory evoked potential, SSEP)를 주로 이용하는데 MEP는 피질척수로(corticospinal tract), 즉 운동신경로의 변화를 주로 감지하며 SSEP는 척수뒤기둥(dorsal column), 즉 감각신경로의 변화를 주로 감지한다[1]. 경추 수술 환자를 대상으로 한 선행연구에서는 MEP와 SSEP를 같이 사용한 복합 감시를 적용할 경우, 수술 중 신경 조직의 손상을 감지하고 수술 후 신경학적 합병증을 예방하는 데 도움이 될 수 있다고 보고하였다[2]. 다른 선행연구에서는 척추 수술 중 IONM의 진폭 증가나 잠시의 감소가 관찰된 경우에 근력과 기능면에서 더 좋은 예후를 보였다고 하며[3], 환자의 주관적인 증상도 호전되었다고 보고하였다[4].
본 논문에서는 경추척수증 환자의 IONM에서 MEP, SSEP 지표의 저명한 호전이 기능적 회복으로 이어진 증례를 상세히 보고하고 이에 대해 고찰하고자 한다.
증례
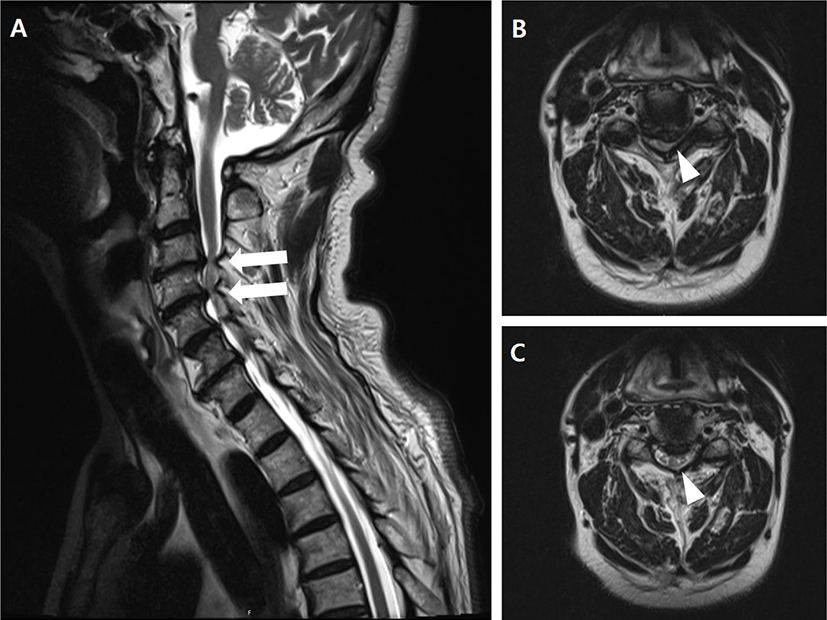
71세 남자 환자가 1년 전부터 시작된 보행장애를 주소로 내원하였다. 환자는 보행 시 균형을 잡기 어렵다고 하였으며 좌측 상지의 근위약, 파행 등의 소견도 함께 호소하였다. 이학적 검사에서 양측 어깨 관절의 외전이 Medical Research Council(MRC) 3등급, 좌측 팔꿈치 관절의 신전과 굴곡이 MRC 4등급으로 측정되었으며 좌측 상지에서 감각 저하가 관찰되었다. 양측 상지의 심부건반사가 항진되었으며, Lhermitte 징후 양성, Hoffman 징후 양성, Babinski 반사 양성 소견이 확인되었다. 근전도 검사에서는 양측 삼각근 삼각근(deltoid) 및 우측 상완 이두근(biceps brachii)의 비정상 자발전위와 동원의 감소가 나타나는 양측 경수 5번 신경근병증 시사 소견이 관찰되었고, 경추 자기공명영상 검사에서 경추3/4번, 경추 4/5번 추간판이 탈출되어 척수를 압박하는 소견이 관찰되었다(Fig. 1). 이에 증상의 악화를 막기 위해 전방 경유 경추체 유합술을 시행하기로 하였다.
마취는 프로포폴(propofol)과 레미펜타닐(remifentanil)을 사용하여 완전정맥마취(total intravenous anesthesia) 방식으로 진행되었다. 기관 삽관 전 근이완제 로쿠로늄(rocuronium) 50 mg이 1회 정맥주사되었고, 이후에는 사용되지 않았다. IONM은 NIM-ECLIPSE System® 4 (Medtronic Xomed, Jacksonville, FL, USA) 장비를 통해 이루어졌으며, MEP, SSEP, train of four(TOF)와 자발근전도(spontaneous electromyography)를 이용하였다. MEP는 두개경유전기자극(transcranial electrical stimulation) 방식으로 C3-C4 위치에서 450 volt의 5번 반복 펄스로 자극하였으며, 양측 삼각근(deltoid), 노쪽 손목 굽힘근(flexor carpi radialis), 짧은 엄지 벌림근(abductor pollicis brevis), 전경골근(tibialis anterior), 엄지 발가락 벌림근(abductor halluces)에서 기록하였다. SSEP는 양측 정중신경(median nerve)과 경골 신경(tibial nerve)에서 25 mA의 강도로 4.91 Hz의 주기로 자극하고 C3’-C4’에서 기록하였다. TOF는 양측 경골신경을 자극하여 엄지 발가락 벌림근에서 기록하였다. 자발근전도는 양측 삼각근, 노쪽 손목 굽힘근, 짧은 엄지 벌림근, 전경골근, 엄지 발가락 벌림근에서 기록하였다.
유도(induction) 후 TOF 4/4인 상태에서 SSEP와 MEP의 기준값(baseline)을 얻었다. 좌측 전경골근과 우측 짧은 엄지 벌림근에서는 MEP 파형이 형성되지 않았으나 다른 부위의 MEP와 SSEP에서는 파형 형성이 잘 이루어졌다. 수술 시작 33분 후 좌측 노쪽 손목 굽힘근, 전경골근, 양측 엄지 발가락 벌림근에서 MEP의 진폭이 크게 증가하였다. 이중 좌측 엄지 발가락 벌림근은 수술 중 기준값 진폭의 1,235%까지 상승하였으며, 다른 근육들도 진폭에서 증가를 보였고 수술 종료까지 기준값에 비해 증가한 진폭이 유지되었다(Fig. 2). MEP의 잠시는 진폭이 갑작스럽게 증가하는 수술 시작 33분 후에는 큰 변화가 없었으나, 수술 종료 시에는 기준값에 비해 양측 엄지 발가락 벌림근에서 약 10%의 감소를 보였다(좌측 48 ms → 43.5 ms, 우측 51 ms → 45 ms). SSEP는 수술 중 파형이 유지되었으며, 수술 종료 시 양측 정중신경 N20과 후경골신경 P37 파형의 잠시가 기준값에 비하여 약 10% 정도 감소한 소견을 보였다(Fig. 3).
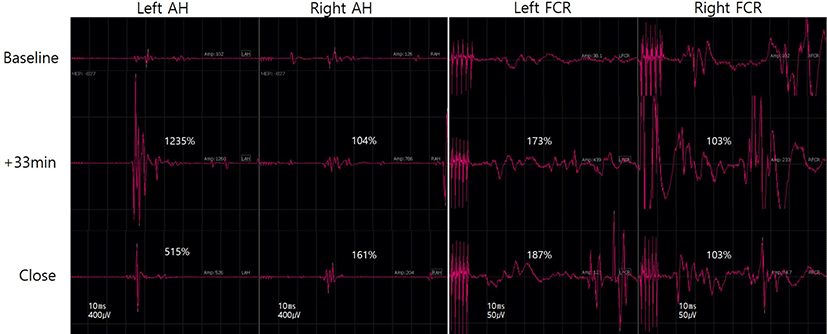
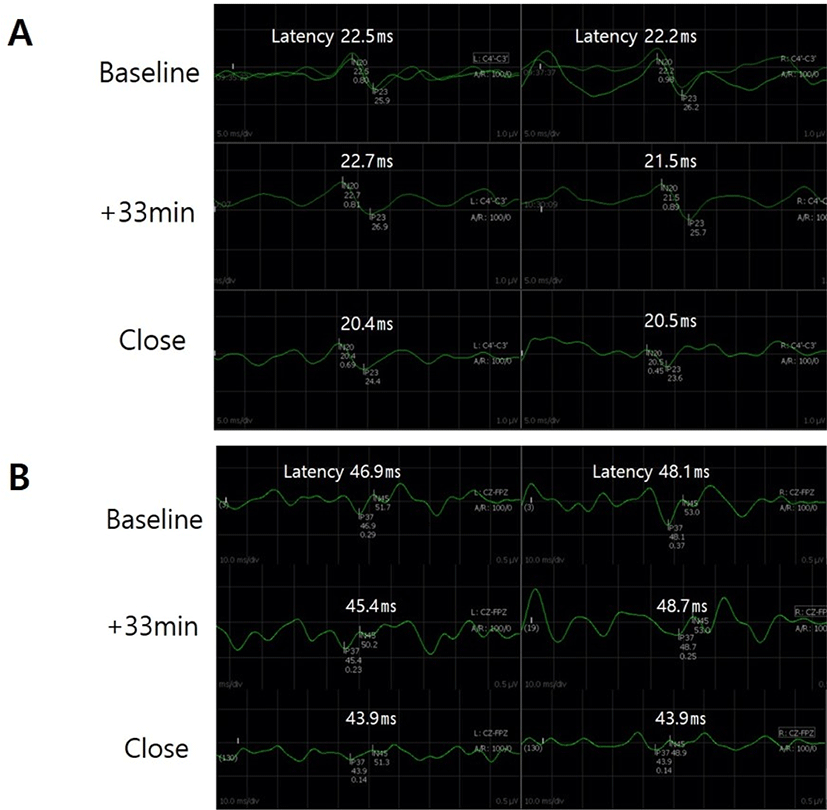
퇴원 시에는 양측 어깨 관절의 외전이 4등급, 팔꿈치 관절의 굴곡이 5등급으로 호전되었다. 수술 한달 후에는 다리 떨리는 것이 없어졌다고 표현하며 보행장애가 호전되었다고 하였고, 좌측 상지의 감각저하가 수술 전에 비해 호전되었다.
고찰
경추척수증은 경추의 퇴행성 변화로 척수에 압박이 가해지면서 발생하는 신경학적 질환으로 자연적으로 회복되기보다 진행하는 양상을 보이기 때문에 수술적 치료를 하는 것이 권장된다. 전방 경추 감압술의 경우 척수의 운동 경로에 가까운 방향으로 접근하기 때문에 수술 중 신경 조직의 손상에 유의해야 한다. 이때 IONM는 수술 중 신경 조직의 손상을 감지하고 조치를 취하여 비가역적인 손상을 방지하는 데 도움을 줄 수 있다[5].
척추 수술의 IONM에서 MEP와 SSEP는 가장 기본적인 검사이며, 많은 연구에서 MEP가 SSEP에 비해 민감하다고 알려져 있다. 특히 경추 수술에서 전방 접근법을 시행할 때 피질척수로를 주로 반영하는 MEP가 SSEP보다 신경 조직의 변화를 더 민감하고 빠르게 발견할 수 있다[1]. 그러나 척추 수술에서 MEP 단독 검시는 복합 감시와 비교했을 때 민감도와 특이도가 낮고[2], MEP의 파형 형성이 되지 않는 등의 경우에는 MEP 단독으로는 IONM을 효과적으로 수행할 수 없다[6]. 본 증례에서 수술 후 33분경 MEP의 갑작스러운 진폭 증가가 관찰된 후 SSEP의 잠시가 점진적으로 감소된 것은 이런 선행연구를 뒷받침하는 것으로 보인다.
몇몇 선행연구에서는 IONM 지표의 호전이 좋은 예후를 시사한다고 보고하였다. 경추척수증 환자의 수술 중 진폭이 50% 이상 증가하거나 잠시가 10% 이상 감소하는 ‘양성 변화(positive changes)’가 있을 경우 근력과 기능 등에서 좋은 예후를 보인다고 보고하였으며[3], 척추 수술에서 IONM의 지표가 호전되었을 때 근력과 함께 환자의 주관적 증상이 호전된다는 연구 결과도 발표되었다[4]. 이는 IONM이 신경학적 합병증의 예측과 방지에 그치지 않고 신경 조직의 회복과 수술 후 예후도 평가할 수 있음을 의미한다. 본 증례에서는 IONM에서 MEP의 진폭 증가, 잠시의 감소와 SSEP의 잠시의 감소가 관찰되었으며, 수술 후 양 상지의 근력, 보행장애 및 감각저하가 호전된 양상을 보였다. 이는 경추척수증에서 척수의 신경조직은 가역적으로 손상된 것이며 기계적인 압박이 해소되었을 때, 신경의 전도 또는 피질척수로(corticospinal tract)의 흥분성이 향상되고 즉각적인 MEP 진폭의 증가로 이어진다는 선행 연구를 뒷받침한다[4,7]. 척수 압박 환자의 수술에서 뇌척수액(cerebrospinal fluid)의 정체와 그에 따른 압력이 해소되면서 즉각적으로 MEP의 호전이 관찰되었고, 이후 신체 진찰과 자기공명영상에서 회복 소견이 관찰되었다는 증례도 IONM을 통해 신경 조직의 회복을 예측할 수 있다는 것을 보여준다[8]. 본 증례에서는 SSEP에서 유의미한 호전이 보이지 않았던 선행 연구와 달리[3], 점진적인 SSEP 잠시의 감소가 관찰되었다. SSEP에서 일시적인 변화를 보인 환자와 지속적인 변화를 보인 환자들을 비교했을 때, 지속적인 변화를 보인 환자에서 신경학적 합병증의 빈도가 높았다는 연구 결과를 고려하면[9], 해부학적으로 취약한 척수뒤기둥에도 가역적으로 손상된 부분이 있을 수 있으며, SSEP는 이런 신경 조직의 회복을 반영한다고 유추해 볼 수 있다.
퇴행성 경추척수증에서 척수의 압박이 계속되면 회백질의 괴사와 탈수초화가 진행되어 비가역적인 손상으로 이어지고, 따라서 증상의 지속기간이 길어질수록 수술 후에 좋은 예후를 기대할 수 없다고 알려져 있다. 그러나 외래에서 보존적 치료 후 증상이 악화되었을 때 수술을 시행한 환자들에게서 증상의 지속기간은 수술 후 임상적 호전과는 연관이 없다는 선행 연구도 보고되었다[10]. 본 증례에서는 증상이 1년 동안 지속되었음에도 불구하고 IONM 지표와 수술 후 임상 증상의 호전이 관찰되었는데, 이는 만성적인 경추척수증에도 수술적 감압으로 회복을 기대할 수 있음을 의미한다.
MEP와 SSEP에 영향을 줄 수 있는 요인으로 수술 중 신경조직의 변화 외에도 기계의 오류, 환자의 체온, 혈압, 산소포화도 또는 체위의 변화, 마취심도와 마취약제, 근이완제의 영향 등을 고려할 수 있다. 전신인자에 의한 유발전위의 변화는 서서히 진행하는 경우가 많고, 수술이나 허혈에 의한 신경 손상, 체위 변경으로 인한 신경의 압박은 갑작스러운 유발전위의 변화를 보이는 경향이 있다. 본 증례에서 관찰된 MEP의 진폭 증가는 수술 중 갑작스럽게 나타났으며, 이후 임상적으로도 근력의 호전을 보였기에 전신 인자에 의한 것보다는 신경 조직에 가해진 압박의 해소에 의한 것으로 보인다.
결론적으로, 경추 수술에서 IONM은 신경학적 합병증뿐만 아니라 신경 조직의 회복도 예측할 수 있으며 이때 단독감시보다는 복합감시가 우월하다. IONM 지표 호전의 임상적인 의미를 정확히 알기 위해서는 수술 전후에 상세한 검사가 필요하며, 추후 보행분석 또는 근전도 등의 객관적이고 자세한 평가 방법을 이용한 전향적 연구가 필요하다.







