서론
수술 후 신경학적 손상을 예방하기 위해 수술중신경계감시(intraoperative neurophysiological monitoring)가 시행된다. 척추 수술에서는 운동유발전위(motor evoked potentials, MEP), 체성감각유발전위(somatosensory evoked potentials, SEP)의 감시를 통해 감각신경로와 운동신경로를 연속적으로 감시하여 척수 및 척추신경근 손상의 위험요인을 조기에 발견하여 수술 후 합병증을 방지하기 위해 수술중신경계감시를 시행한다[1].
수술중신경계감시는 일반적인 신경생리검사와 비교하였을 때 수술실이라는 특수한 환경에서 수술 환자를 대상으로 진행하는 검사이기 때문에 환자의 자세나 생체 징후, 마취 상태 등 다양한 외부 요인이 작용할 수 있고 이에 의해 유발전위 파형이 변화할 수 있다.
모니터링 중 발생한 이상 소견이 실제 신경 손상으로 인한 것인지 외부 요인에 의한 체내 변화에 의한 것인지 혹은 기기의 단순 오류에 의한 것인지를 구별하는 것이 매우 중요하다[2]. 수술 부위에 이뤄지는 직접적인 수술 행위와 관련된 변화로 생각될 경우, 수술의와의 적극적인 대화를 통해 수술을 잠시 멈추고 관찰하거나, 현재 수술 과정이 신경 손상을 유발할 가능성이 있는지 확인하는 등의 과정이 필요하겠다. 환자 체온 및 혈압의 변화, 마취 심도 및 마취제 종류의 변화, 환자 체위 등이 변했는지 등을 마취의, 수술의와 함께 상황을 공유하는 것이 중요하다.
본 증례는 경추 수술 환자에서의 경추 견인 및 자세 변화, 손목 압박에 의해 발생한 수액 공급 장애로 인한 혈압 저하가 수술중신경계감시에 미치는 영향에 대해 논의하고, 수술중신경계감시를 통해 수술 중 자세의 이상 및 혈역학적 이상 소견을 조기에 발견하여 교정하는 것이 수술 후 좋은 예후로 이어짐을 강조하고자 한다.
증례
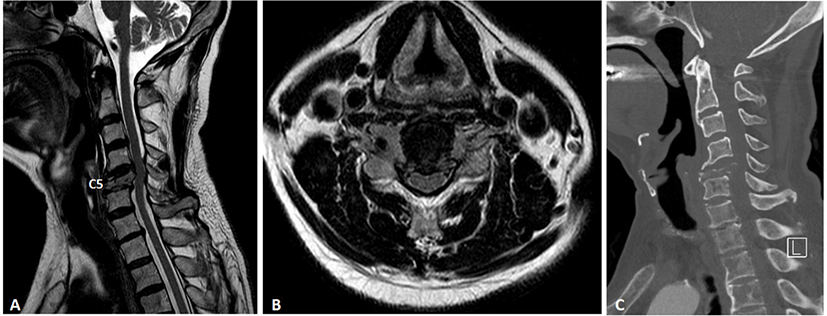
본 72세 남성은 관상동맥 폐쇄성 질환, 당뇨병, 전립선암 과거력 있는 분으로 내원 2개월 전인 2022년 3월경부터 경추부 통증 및 양측 상지 위약감 증상이 발생하였다. 이에 타 병원에서 시행한 경추부 자기공명영상 검사상 경추 5번 병적 골절 및 동일 위치의 척수 병증 소견이 확인되어 본원 정형외과에서 수술적 치료를 위해 내원하였다(Fig. 1-A, Fig. 1-B). 본원 내원 당시 시행한 신경학적 검사상, 양측 상지 근력 저하 소견 보였고 감각 저하 소견은 없었으며, 양측 팔과 손에 저린 증상을 호소하였다. 자기공명영상에서 경추 5번 척수의 압박이 심하고 신경학적 증상이 동반되어, 환자의 증상을 개선하고 추가적인 신경손상을 예방하고자 수술적 치료를 계획하였다. 수술 5일 전 추가적으로 시행한 경추부 컴퓨터단층촬영 검사상, 경추 5번 위치에 병적 골절과 척추의 다발성 뼈 전이 소견이 확인되었다(Fig. 1-C). 수술은 1차적으로 경추 3, 4, 5, 6, 7번 후방 경추 유합술을 진행하고, 이틀 후 2차 수술로 전방 경추 5번 추간판 제거술 및 경추 4, 5, 6번 유합술을 진행하기로 하였다. 환자는 수술 전 기초 검사로써 SEP, MEP를 포함한 전기진단학적검사를 시행하지 못하였다.
1차 수술 시, 수술중신경계감시를 시행하였으며, MEP, SEP와 fEMG(free running electromyography)를 지속 감시하였다. MEP는 양측 대뇌 운동범위 피질을 C1-C2와 C3-C4 몽타쥬에서 300–400 V 강도로 0.05 msec 동안 3.0 msec 간격으로 자극하여 양측 삼각근(deltoid), 단무지외전근(abductor pollicis brevis), 앞정강근(tibialis anterior), 엄지벌림근(abductor hallucis)에서 기록하였다. 정중신경 SEP는 양측 손목의 정중신경을 12–15 mA의 강도로 0.3 msec 동안 4.7 Hz의 주기로 자극하고 C3’-C4’ 몽타쥬로 기록하였다. 뒤정강신경 SEP는 양측 발목의 뒤정강 신경을 16–20 mA의 강도로 0.3 msec 동안 4.7 Hz의 주기로 자극하고 Cz’ 몽타쥬로 기록하였다. MEP는 기저파형 대비 50% 이상의 진폭 감소가 있을 경우, SEP는 기저파형 대비 50% 이상의 진폭 감소 혹은 10% 이상의 잠시(latency) 증가가 있을 경우를 경고기준(alarm criteria)으로 사용하였다. 양측 삼각근과 단무지외전근, 앞정강근, 엄지벌림근에서 fEMG를 지속적으로 관찰하였다. 7:55: 04 마취 시작하였고 수술 시 환자는 앙와위(supine position)에서 전신마취를 시행하고, 기관내 삽관 이후 복와위(prone position)로 체위를 변경하였다. 복와위 상태에서, 환자의 양 팔은 몸통에 완전히 붙인 상태로 벨트로 고정되었다.
7:55:04에 마취를 시작하였고, 수술 시 환자는 앙와위(supine position)에서 전신마취를 시행하고, 기관내 삽관 이후 복와위(prone position)로 체위를 변경하였다. 수술중신경계감시 세팅 직후인 8:47:22에 양측 정중신경에서, 8:47:24에 양측 뒤정강신경에서 안정적인 SEP 파형을 획득하였으며, MEP 파형은 각각 좌측과 우측의 삼각근과 단무지외전근, 앞정강근, 엄지벌림근에서 8:45:08 및 08:45:13에 기저 파형을 안정적으로 획득하였다.
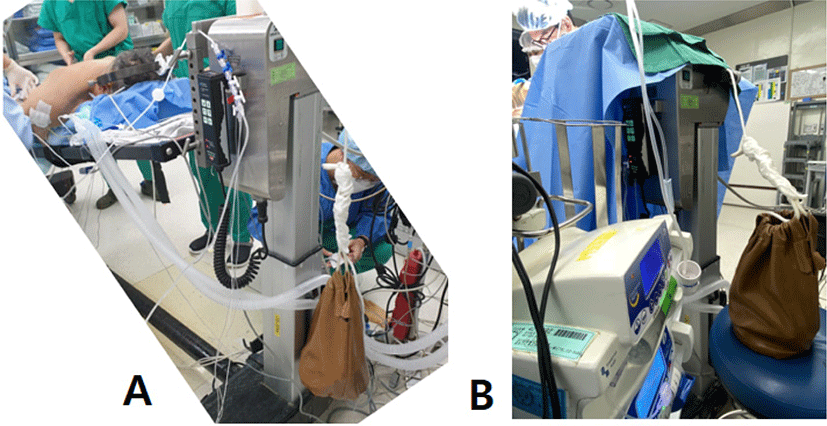
수술 시작 후 9:21:22 시점에서 갑자기 우측 정중신경에서 SEP 10% 이상의 잠시 증가가 확인되었고 기준 파형 세팅 후부터 40분간 정중신경에서 SEP 진폭 감소가 점진적으로 나타나다가 9:48:21 시점에서 우측 정중신경에서 SEP 50% 이상의 진폭 감소가 확인되어 수술의에게 보고되었다(Fig. 2). 그와 동시에 좌측 정중신경은 경고 기준을 경고기준에는 미치지 못 하였으나 약 SEP 7%의 잠시 증가 및 약 20%의 진폭 감소된 소견이 확인되었다. 세팅 직후 기준 파형의 SEP 파형이 안정적으로 관찰되었고 양측 뒤정강신경 SEP에서 이상소견이 확인되지 않았던 점을 미루어 봤을 때 전신적인 환자 상태 때문이 아닌, 국소적인 문제로 생각되어 수술의 및 마취의와 논의하여 환자의 혈역학적 상태, 장비 및 환자 자세를 포함한 주변 환경을 점검하였다. 환자는 골절로 인한 척수 압박 있어 수술 시야 및 공간 확보를 위해 복와위 자세에서 7 kg의 추를 이용하여 경추를 견인하고 있는 상태였으며, 경추 굴곡이 SEP 변화의 원인일 가능성을 고려하여, 수술의와 상의하여 9:31: 19에 경추 견인을 모두 해제 후 수술을 시작하였다(Fig. 3). 자세 변경 이후 우측 정중신경 SEP 회복이 서서히 보이기 시작하였으나 경고 기준에서 벗어날 정도로 회복되지 않았고, 10:02:27 시점에서 환자 수축기 혈압(systolic blood pressure, SBP)이 83 mmHg, 이완기 혈압(distal blood pressure, DBP)이 38 mmHg, 평균동맥압(mean arterial pressure, MAP)이 53 mmHg로 저하된 것을 확인되었다. 관상동맥 폐쇄성 질환이 있던 환자로 혈압 조절에 어려움이 있을 위험도가 높았던 환자라, 기저질환에 의한 혈압 변동으로 생각하여, 마취통증의학과에서 ephedrine(EPHEDrine, Jeil, Seoul, Korea) 2 mg 정맥 주사 시행하였으나 혈압이 회복되지 않아 환자 주변 환경을 재점검하였고, 우측 정맥 주사 라인이 환자의 손목에서 조여진 벨트에 의해 압박된 상태로 발견되었다. 이에 압박 상태를 해결한 후 SBP 140 mmHg, DBP 63 mmHg, MAP 87 mmHg로 회복이 되었고 우측 손목의 감압 후 약 5분 후인 10:01:58 시점에서 우측 정중신경 SEP가 기준파형의 6% 잠시 증가, 기준파형 이상으로 진폭이 회복되어, 경고 기준을 벗어나지 않는 수준으로 회복되었다.

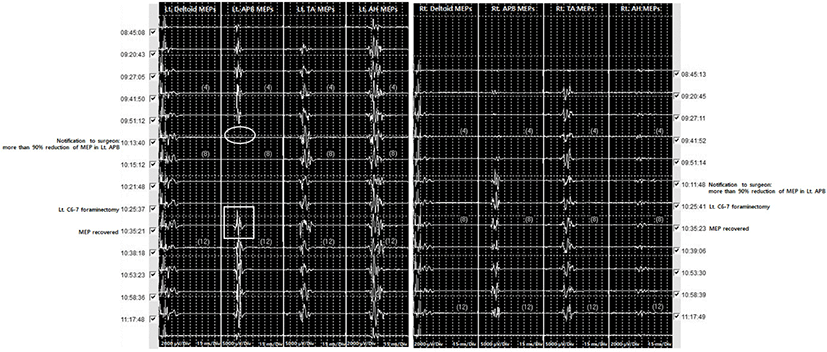
이후, 수술 진행 중, 10:13:40 시점에서 좌측 단무지외전근 MEP의 진폭이 기저파형 대비 90% 이상 저하 소견이 확인되어 수술의에게 보고하였고, 당시 좌측 경추 6-7 추간공 부위에 지혈을 위해 본왁스(bone wax)를 채워넣은 상태였다(Fig. 4). 보고를 받은 수술의는 좌측 경추 6-7 추간공 절제술(C6-7 foraminectomy)을 빠르게 시행하였으며, 10:35:21에 좌측 단무지외전근의 MEP 진폭이 경고 기준 이내로 회복하였다. 이후 SEP, MEP 모두 경고 기준 이내로 회복된 것을 확인하여 10:25:58에 수술 시야확보를 위해 다시 경추 견인(7 kg)을 시행하였다. 그러나 10:34:06 정중신경 SEP의 잠시가 10% 이상의 잠시 증가, 10:39:30 우측 정중신경 SEP의 잠시 증가 소견이 확인되어 수술의 및 마취의와 논의하였고, 경추 견인을 7 kg에서 5 kg로 감량하였다. 이후 좌측 정중신경 SEP의 잠시 증가는 경고 기준을 벗어나지 않는 수준으로 회복하였으며 좌측 정중신경 SEP의 잠시 증가는 점진적으로 회복되었으나 경고 기준 이내로는 회복되지 않아, 수술 종료 시 기준파형에 비해 10.6%의 지연을 보였다.
수술 2일 후 시행한 신경학적 검사상, Medical Research Council(MRC) Scale for Muscle Strength 기준으로 상지 근력은 4점에서 5점으로 호전된 양상 보였고, Japanese Orthopedic Association(JOA) score는, 수술 전 15점(17점 만점; 양측 팔과 손의 근력 저하 소견 보여 2점 감점)에서 수술 후 1개월, 3개월째 모두 총점 17점으로 회복되었다.
고찰
척추 수술 시 척수 및 척추신경근이 눌리는 가능성이 있는 상황에서 과도하게 경추가 견인된 상태를 유지할 경우 신경 손상을 진행시킬 가능성이 있기 때문에 적절한 수술 자세를 유지하고 적절한 견인 무게를 적용하여 척수 신경의 과신전 및 눌림을 유발하는 자세를 피해야 한다. 척추 수술 시행 중 과도한 경추의 굴곡과 같은 자세 이상으로 인한 수술중신경계감시 이상 소견을 확인하여 사전에 신경 손상을 예방할 수 있었던 증례들이 보고된 바 있다[3–5]. 본 증례에서는 수술 중 과도한 경추 견인으로 인한 전기생리학적 이상을 수술중신경계감시를 통해 조기에 발견하여 환자의 신경계 손상을 예방할 수 있었던 증례로, 경추 견인 무게를 줄이고 난 이후 점진적으로 SEP 파형이 회복되는 양상을 확인할 수 있었다.
잘못된 체위 또한 말초신경의 손상을 일으켜 유발전위 검사결과에 영향을 미칠 수 있다[6]. 본 증례에서는 환자의 마취가 완료된 시점에 빠르게 수술중신경계감시 세팅을 완료하고, 세팅 직후에 SEP의 기저파형을 획득하였으며, 체위 변경 이전부터 SEP 파형을 지속적으로 모니터링하였기 때문에 파형 이상이 감지된 순간 수술에 참여한 모든 의료진과 상황을 빠르게 공유할 수 있었다. 또한 양측 뒤정강신경 SEP에서 이상소견이 확인되지 않았던 점을 미루어 봤을 때 전신적인 요인보다는 국소적인 문제의 가능성이 높다고 판단하여 마취의와 수술의와 긴밀하게 소통하여 원인을 파악하고 교정하여 신경계 손상을 예방할 수 있었다.
또한, 수술중신경계감시는 척추의 과도한 신전과 같은 직접적인 중추신경에 영향을 끼치는 요인 외에도 말초신경, 환자의 혈압, 출혈 여부를 포함한 혈역학적 상태, 체온, 마취 상태 등의 전신 상태를 포함한 여러 요인들이 있다. 본 증례에서 우측 정맥 주사의 압박으로 인한 혈압 저하의 회복이 지연되어 발생한 SEP 저하에 대한 증례였다. 환자의 수액 라인은 우측 손목에서 압박되어 있어, 수액 및 승압제가 원활하게 공급되지 못하는 상황이었다. 평균 동맥압이 80 mmHg 이하로 떨어질 경우 SEP의 진폭 감소를 유발하며 검사의 신뢰도를 저하시키기 때문에, 유발전위의 이상 소견이 있을 경우 수술의뿐 아니라 마취의와 함께 환자 상태를 빠르게 점검해야 한다[7].
더불어, 수술중신경계감시뿐만 아니라 일반적인 전기신경학적 검사에서도 체온 감소 시 점진적인 서파 증가 및 진폭 감소를 보이는데, 수술실 내부는 계절과 상관없이 낮은 온도(20℃–24℃)로 유지하고 있어, 장시간의 수술로 인한 중심 및 말초 체온의 저하가 발생하기 쉽다. 그러나, 본 증례에서는 환자의 체온을 유지하기 위한 장치(forced-air warming blanket)를 사용하였고, 수술 과정 내내 환자의 체온을 적정하게 유지하였다. 차가운 생리식염수로 수술 부위를 지속적으로 세척하는 경우에도 유발전위 변화를 일으킬 수 있으나 본 증례에서는 따뜻한 생리식염수를 사용하였으며, 세척 빈도가 잦지 않아 유발전위 변화의 원인은 아니었다.
수술 전 SEP 및 MEP를 포함한 전기진단학적 검사를 시행하지 못한 것은 본 증례의 제한점이다. 환자는 수술 전 양측 상지의 근력 저하가 있었으나, 양측 상지의 저린 증상 이외의감각 저하 소견은 보이지 않았고, 수술중 SEP와 MEP의 기저파형이 모니터링 가능한 수준으로 확인되었으나, 수술 전 SEP와 MEP 파형 정보가 누락되어 있어, 환자의 전기생리학적 상태를 수술 전과 비교하기는 어려웠다는 한계점이 있다. 수술중신경계감시의 이상소견을 빠르고 정확하게 판단하기 위해서는 수술 전 전기진단학적 검사를 시행하여 환자의 전기생리학적 상태를 확인하는 것이 중요하다. 더불어, 수술 전 전기생리학적 상태는 수술중신경계감시의 설계 시 주요 참고사항이 될 수 있으므로 가능한 검사를 시행하는 것이 좋겠다. 본 증례는 수술중신경계감시를 통해 환자 자세 이상 및 혈압 저하의 원인을 조기에 확인하고, 자세와 팔의 압박으로 인한 수액 공급 장애를 신속하게 교정하여 신경계 손상을 예방한 증례이다. 수술중신경계감시 중 이상 소견이 발견되면 수술실 내 모든 의료진들과 신속하고 정확하게 상황을 공유하고 의사소통을 통해 적절한 조치를 취하는 것이 환자의 예후 결정에 중요하겠다.







